|
值得注意的是,不少上市集资的生物制药公司上市时仍处于研发阶段,由于仍未能实现产品商业化,产品能否研制成功亦是未知之数,公司实际的盈利能力存在一定的不确定因素。但反观复宏汉霖坐拥国内首款商业化生物类似药HLX01(汉利康)、可在近年内变现的数款核心产品及潜力巨大的丰富产品管线,此次上市却可谓适逢其时。
多项产品临近商业化 首发布局领先市场
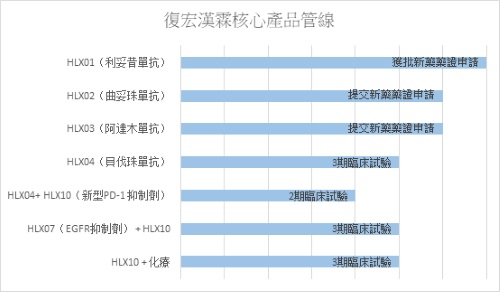
正如上述,复宏汉霖于生物类似药,特别是单克隆抗体领域的进展于国内首屈一指。复宏汉霖旗下的HLX01(汉利康)利妥昔单抗注射液为全国首家根据现行有关评价及上市审批的法规获批上市的生物类似药,已于本年度的5月正式推出市面,并开始产生收入及利润。另外HLX02已于本年度6月获得欧洲药品管理局上市申请受理,成为中国首个在欧盟报产的国产单抗生物类似药,同时是首个被欧盟受理的「中国籍」曲妥珠单抗 。同时,复宏汉霖另外多款的核心药品现亦处于临床研究的后期阶段,临近正式商业化。
由此可见,复宏汉霖现正适逢十年以来的研发投入陆续转化为成果的阶段,多款产品临近踏上商业化征程。随着产品销售,公司也将逐渐产生收益:其中利妥昔单抗已被列入国家医保目录及国家基本药物目录。根据市场研究报告预计,于2020年,复宏汉霖HLX02-04三款接近商业化的产品,连同已实现商业化的HLX01于国内的总市场规模将达人民币167 亿元。
复宏汉霖其中一项最明显的优势在于其研发的效率,其中HLX01及02更是领先了后续的其他竞争对手近一年半时间。于这段期间,复宏汉霖积极布局市场,并通过国际化战略合作力争开拓海外市场。据悉,复宏汉霖现已与Accord、Cipla、Biosidus 、雅各臣药业及KG Bio等多家知名制药企业订立协议,于全球92个国家和地区,包括欧洲、澳大利亚、香港及马来西亚等多个市场中推广及分销其产品,为全球更多患者带来切实的获益。
庞大产品线助研联合治疗 借势类似药进军创新疗法
虽然复宏汉霖率先在单抗生物类似药的领域拥有较大的先发优势,但据其招股书披露,生物类似药并非复宏汉霖的唯一研发方向,公司同时亦基于生物类似药的开发优势,逐步推进创新型单抗产品及联合疗法的开发,从而构建成一个全能型的平台。
复宏汉霖旗下HLX10(重组抗PD-1人源化单抗产品)已于美国、中国台湾及中国大陆获得新药临床试验申请批准,可用于多种实体瘤的治疗,现单药已进入2期临床试验阶段,正进一步探索其用于治疗慢性乙型肝炎的可能性。此外,复宏汉霖围绕自主开发的抗PD-1和PD-L1,和联合产品线中丰富的产品推出免疫联合疗法。目前公司已陆续就HLX10与自有产品HLX04(贝伐珠单抗生物类似药)、HLX07(重组抗EGFR人源化单克隆抗体注射液)等单抗以及化疗联用开展多项肿瘤免疫联合疗法。
据复宏汉霖管理层日前于全球发行新闻发布会上披露,公司各项产品的研制工作进展顺利,于未来数年年内,公司的多款产品包括HLX02-04以及HLX10亦将陆续推出市面。据招股书披露,复宏汉霖是次全球发售的所得款项,除10%作为营运资金及一般企业用途外,其余大部份的款项均将用于推进各项药品的临床试验、监管备案及注册之上,以开发更多高质的产品。